un dipôle) par lequel cette molécule pourrait se retenir à la phase stationnaire: l'alumine qui elle, est hérissée de dipôles. Al est à l'état Al3+ et les oxygènes à l'état de O2-.
Ne pouvant s'accrocher à la phase stationnaire, il est entraîné rapidement par l'éluant dans lequel il est, de plus très soluble. L'éther de pétrole est un hydrocarbure.
l'affinité (ester: 2 atomes O dans la molécule), elles veulent bien se laisser entraîner.
Ether de pétrole = C6H14 grosso modo ce n'est pas du tout un éther. Il s'évapore aussi vite que l'éther des pharmacies ...

1 première étape.
a) l'éthanol absolu absorbe l'eau des cellules de l'épinard. On ne le garde pas.
b) le dichlorométhane CH2Cl2 dissout les colorants: chlorophylle et carotène ... et sans doute d'autres espèces chimiques non colorées.
C'est une protection ostentatoire pour faire voir combien-le-chimiste-est-respectueux-de-l'environnement !
2 la chromatographie sur colonne.
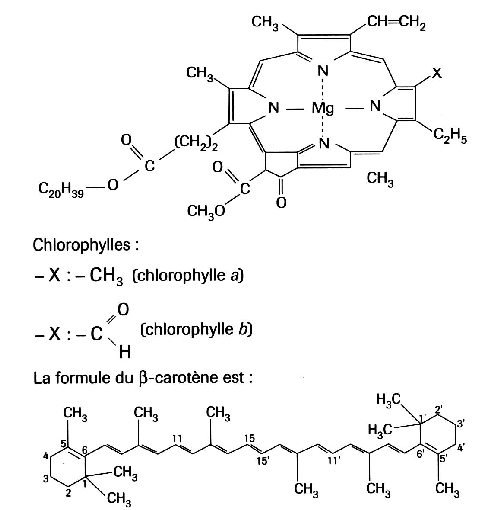
le b-carotène est un hydrocarbure: il ne possède pas de site pôlaire (possédant un défaut ou un excès de charge électrique créant