A) Le tableau d'avancement d'une réaction est un outil puissant et sûr. Il oblige à tout écrire et grâce à cela, on n'oublie rien en cours de raisonnement.
Il met clairement en évidence la valeur maximale, permet de trouver non seulement les quantités de matière des produits mais aussi les quantités de matière des réactifs en excès.
B) Le lecteur aura compris que les calculs de quantités de matière, en chimie, ne peuvent traiter que des moles.
A partir des quantités de matière, on peut atteindre tout le reste:
les masses car mX = nX . Mx
les volumes pour les gaz, si ils sont assez proches de la perfection, par la loi du gaz parfait:
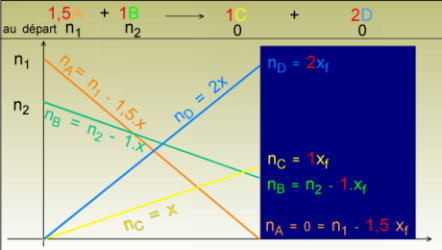
VX = nX. RT/P de toute manière c'est la seule équation des gaz dont on dispose au Lycée! Pour les esprits qui n'ont pas peur des courbes, on peut représenter les graphes des contenus des quantités de matière en fonction de x:
D) Le mode d'emploi est toujours le même
