Selon la zone de pH à surveiller (pendant un dosage par exemple) on choisira un indictateur coloré plutôt qu'un autre.
Les indicateurs sont des couples acide base dont chaque forme a une couleur différente.
Cela veut dire que par leur système de liaisons moléculaires conjugué ils absorbent dans le spectre visible
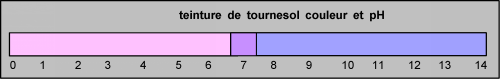
dans la zone du virage la couleur est le mélange des deux teintes: la teinte acide et la teinte basique.
Il s'agit de couleurs, synthèse soustractive !!!
la protonation du système conjugué modifie la fréquence de résonnance et change leur courbe de transmission. Cela change donc aussi le spectre de la lumière transmise vers notre oeil: leur couleur change.
Lorsque l'indicateur est dans un pH = pKa les deux formes coexistent à égalité: la couleur est celle du mélange de la forme acide et de la forme basique de l'indicateur.
A pH = pKa -1 il y a 10 fois plus de forme acide: c'est la teinte de la forme acide de l'indicateur que l'on voit. A pH = pKa + 1 on ne voit que la couleur de la forme basique.
indicateurs au laboratoire
