A: Voici plusieurs noyaux d'atomes qui portent tous le même nom: le nom de l'élément auquel ils appartiennent:
le CUIVRE.
Ils ont une caractéristique qui les différencie les uns des autres:
Ils n'ont pas la même masse. Comme ils sont tous du cuivre, ils ont le même nombre de protons.

C) par définition:
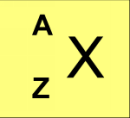
A est le nombre de masse.
Z est le numéro atomique.
Z détermine de quel élément il s'agit, il décide aussi du nombre d'électrons qui peuplent l'atome. C'est le même nombre car les atomes sont électriquement neutres.
A est obtenu en ajoutant le nombre Z et le nombre de neutrons.
D) deux nucléïdes sont isotopes lorsqu'ils ont même Z et des nombres A différents.
Comme c'est le nombre d'électrons qui commande la réactivité chimique, deux isotopes ont strictement le même comportement dans les réactions chimiques.
Il n'est pas facile de les séparer!
B: alors c'est qu'ils n'ont pas le même nombre de neutrons. Les six nucléïdes représentés sont isotopes.
On note chaque nucléïde par le symbole
complet : ...