Il faut placer six G.E.D. autour de l'atome central. La structure de l'OCTAÈDRE est celle qui propose les angles les plus grands
Mais nous avons combiné les six orbitales, on parle d'hybridation. Ainsi, elles ont le même état énergétique. Qu'en dit Schrödinger?
Il faut placer six G.E.D. autour de l'atome central. La structure de l'OCTAÈDRE est celle qui propose les angles les plus grands

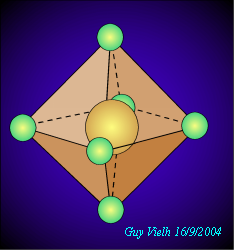 .
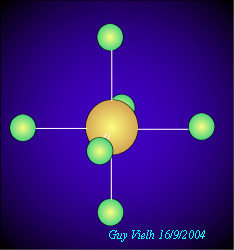
.
Dans le cas de la formation de l'hexafluorure de soufre. Si on laisse le soufre écrit:
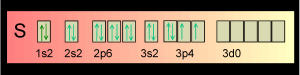
On ne respecte pas la "règle des doubles sièges". Mais cette écriture la respecte:
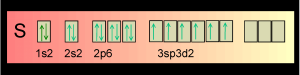
Le soufre sera hexavalent puisqu'il peut échanger six électrons.
En faisant cela, nous avons admis que les orbitales 3s, 3p et 3d avaient le même niveau d'énergie. Lorsque l'atome est dans son état fondamental ce n'est pas vrai.