c) Dans l'exercice 6 on trouve le pKa de NaHCO3 , il vaut 6,4.
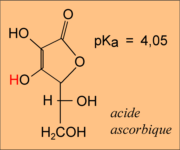
Combien vaut le pKa de l'acide ascorbique ?
pKa = 4,1 on l'appelle HA

Considérons l'acidité de l'acide ascorbique réagissant sur le couple CO2/HCO3-
;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;;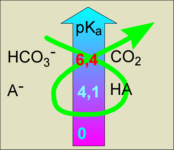 .....................;..................
Bref, hydrogénocarbonate réagit avec l'acide ascorbique
ave dégagement de bulles de CO2: c'est l'effervescence
qui rend si rigolo la prise d'aspirine vitaminée.
.....................;..................
Bref, hydrogénocarbonate réagit avec l'acide ascorbique
ave dégagement de bulles de CO2: c'est l'effervescence
qui rend si rigolo la prise d'aspirine vitaminée.
Qu'est ce que signifie "tamponnée"?
Lorsque la réaction effervescente est finie, il ne reste que le couple HA/A- et log [A-(aq)] / [HA(aq)] + pKa = pH
Cette relation montre que pH ne varie pas beaucoup autour de la valeur du pKa (= 4,1) dans une grande zone autour des concentrations
[A-(aq)] = [HA(aq)] c'est l'effet tampon qui assure que le pH du verre d'aspirine tamponnée est moins acide que celui de l'aspirine seule
b) carbonate CO32- . Monosodique signifie qu'il n'y a qu'un ion sodium Na+ . Tout chimiste distingué doit remarquer que cela ne constitue par la formule d'un sel qui doit être neutre. Il manque un ion 1 fois positif: c'est H+.
Bilan : Na+ , H+ , CO32- = NaHCO3