A) L'exemple industriel est la purification du cuivre.
La métallurgie du cuivre produit du cuivre impur : le blister.
A) L'exemple industriel est la purification du cuivre.
La métallurgie du cuivre produit du cuivre impur : le blister.
B) Le blister est l'anode de l'électrolyse:
Il subit l'oxydation:
Cu = Cu2+ + 2e-
Les éléments comme Ag et Au ne peuvent subir cette oxydation tant que l'élément cuivre existe sous forme d'atomes.
C) Les atomes de cuivre , devenant des ions, quittent l'anode qui est rongée.
Les atomes Ag et Au isolés tombent au fond de la cuve.
L'élément Pb (le plomb) subit l'oxydation car il perd plus facilement deux électrons que Cu. Il tente de passer en solution sous forme de Pb2+.
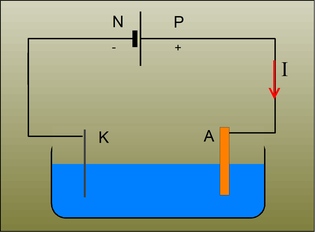
Au bilan, le cuivre est transporté depuis l'anode jusqu'à la cathode. Les impuretés tombent sous l'anode et sont ainsi séparées du cuivre.
D) Cependant, Il se trouve en présence d'ions sulfates avec lesquels il forme un solide insoluble PbSO4 qui tombe aussi au fond de la cuve .
L'electrolyse à anode soluble permet d'éliminer les éléments cités dans cette fiche.
A la cathode, il y a dépôt de cuivre, sans ses impuretés. On obtient le cuivre rouge à 99,99%.
