A) Le silicium est un élément très répandu dans la croûte terrestre.
Comme il est facilement oxydé par le dioxygè,e, il faut renoncer à le trouver à l'état natif.
On trouve son oxyde, la silice, dans le sable (type Fontainebleau) . Très stable, chimiquement, il n'est pas aisé de le réduire à l'état de corps simple.
B) l'intérêt du silicium réside dans le fait que c'est un semi-conducteur: à froid, il ne conduit pas l'électricité mais si on fournit de l'énergie (chaleur, lumière, rayonnements) quelques électrons passent dans la bande électronique de conduction.
Son utilisation la plus célèbre est de constituer diodes, transistors, circuits intégrés, mémoires, microprocesseurs ...
C) tout cela par l'ajout de quantités infimes et contrôlées d'impuretés qui constituent le dopage du silicium.
Il est donc indispensable d'obtenir un silicium d'une extrême pureté avant d'y implanter des atomes "dopants".
On sait produiredu silicium avec un taux d'impuretés de 10-9
On réduit la silice par le carbone vers les 1700°C par électrolyse. Les cathodes sont en carbone et elles sont consommées.
SiO2 + C ---> CO2 + Si
<le silicium ainsi obtenu n'a pas la pureté nécessaire pour ses applications en électronique.
On transforme le silicium en molécules hydrogénées, les SILANES dont voici SiH4 équivalent du méthane en chimie organique:
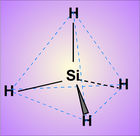
On distille soigneusement les silanes ce qui permet d'atteindre une pureté de 10-5.
On décompose le SiH4 en le déposant en couche plane (dépot épitaxial) qui donne des galettes monocristallines: les WAFERS. Ces plaques seront traitées par les "fondeurs" par bombardements ioniques et microlithographie pour créer les circuits intégrés.
Une autre voie est la formation de SiHCl3 (trichlorosilane), distillation. Réduction par H2 . Le silicium est ensuite fondu dans un creuset et on tire des monocristaux. On purifie ces monocristaux d'environ 200 kg par fusion de zone (c'est une recristallisation fractionnée) . Certte technologie des monocristaux permet de produire du silicium dopé pour certaines applications.
