
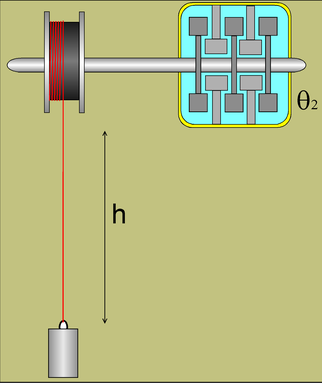
 Dans le calorimètre, on injecte le travail moteur du poids : W
= M . g . h (ce sont des joules)
Dans le calorimètre, on injecte le travail moteur du poids : W
= M . g . h (ce sont des joules)
La température du calorimètre, dont on doit connaître la "masse équivalente en eau" = M' , voit sa température monter de q1 à q2. Cela donne une quantité de chaleur Q = M' . (q2 - q1) (en calories)
Du principe de la conservation de l'énergie, on tire que ces quantités doivent être égales. Cela implique qu'une calorie vaut 4,18 J.
