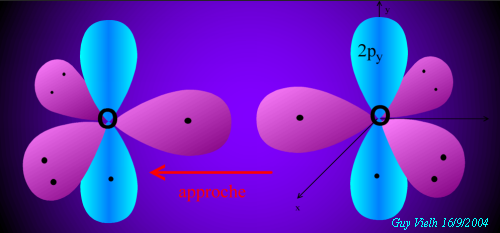

Dans l'exemple montré, cela ne suffit pas à satisfaire la règle de l'octet et UNE AUTRE LIAISON VA SE FORMER entre ces deux atomes.
Mais ceci est une autre histoire à découvrir dans la "liaison p"
Voir la molécule d'éthylène filaire


Une liaison sigma est une liaison covalente dans la plupart des cas. Il s'agit d'un doublet liant entre deux atomes.
Lorsqu'une seule liaison entre ces deux atomes existe, il s'agit d'une liaison sigma.
Si on a une liaison multiple, il y en a une qui est une liaison sigma.
Elle se forme par recouvrement axial d'une orbitale moléculaires de chacun des atomes liés.
Par exemple, entre deux oxygènes, il se forme une liaison sigma. Ce sont les nuages mauves qui se recouvrent.
Ce sont ici des orbitales hybridées. Elles contenaient un électron. La région nommée s forme un seul nuage contenant deux électrons: un doublet liant.