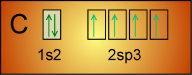
L'atome C possède 6 électrons:
 Structure et représentation de Lewis
Structure et représentation de Lewis
L'atome C possède 6 électrons:

 Structure et représentation de Lewis
Structure et représentation de Lewis
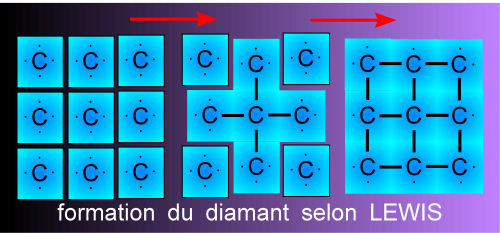
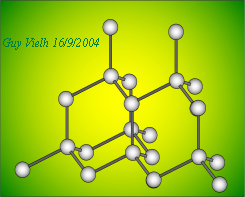
Cela explique: la dureté exceptionnelle du diamant et son incapacité à propager le courant électrique. Il n'existe aucun électron libre ni aucune possibilité de migration d'un trou ou de propagation d'un ion dans une telle structure. Revenir à semi-conducteur.

Le courant électrique est un flux de porteurs de charges qui se déplacent d'un mouvement d'ensemble sous l'influence d'un champ électrique. Cela peut être:
Une matière constituée de molécules ne comportant que des liaisons covalentes ordinaires (non délocalisées) ne peut conduire l'électricité.
Il n'existe dans un tel milieu aucun porteur de charge.
Le cas du diamant montre cela: