1° façon:
Travaillons sur leur ............... structure
de lewis .......... 


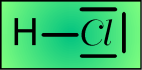
Prenons deux atomes H et Cl.
On peut traiter le problème de trois façons:
elles conduisent toutes au même résultat: la formation d'une liaison covalente entre H et Cl.
3° façon: Traitons la question dans le cadre du modèle ondulatoire:L.C.A.O.
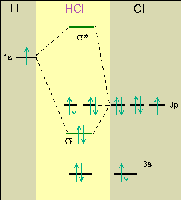
L.C.A.O. = ..... Linear Combination of Atomics Orbitals
2° façon:
Représentons leurs cases quantiques.
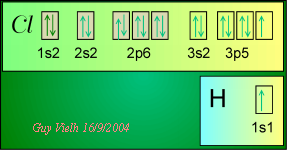
L'électron de H et l'électron impair de la case 3p du Cl vont former un doublet.
Notez bien qu'il existe d'autre liaisons que la liaison covalente:
